�༪��ר�� >> �༪������������III���ٴ��о�
�༪������������III���ٴ��о�
- ��Դ�� �ټ�����ҩ���� ����ʱ�䣺2007-3-13 15:29:00
��I�ں�II���ٴ��о��й۲쵽�ij������������Դ�ʹ������Sorafenib�������������Ժ�ɫ��������ϸ�����ͷ�Сϸ���ΰ���һ�����ٴ�III���о���
����������������������ϸ�����Ģ����ٴ��о�(TARGETs)�������о���ʷ������ģ���������ο�������о������ǻ��������о����,����FDA��2005��12��20�տ�����������������Ϊ������ϸ����������ҩ��,��Ҳ������FDA 13������һ��������������ҩ���һ����ģ�����ٴ�������, ����������ļ�����չ�����ڽϰ�ο�����ӳ���һ��,�ֱ�Ϊ5.8 ��2.8����,�ٴ������ʷֱ�Ϊ84%��55% (P=0.00001),�Ҳ��˵����������������ơ�
Sorafenib������������Ч����Ҫ��һ�������˫ä����ο�����յ�III���ٴ��о����о�11213���ó�����һ��������������о�����Sorafenib ������ֱ�����Ͱ����������ڵ����������������о�100391Ҳ�ṩ�˲������ϡ�
�о�11213
���������˫ä����ο�����յ��ٴ��о��ڹ۲쵽Լ363����չ����Ļ��ߺ��������չ���棨PFS��������Ϊ�˽���PFS����������ָ����һ��ר�ŵ�Ӱ��ѧ���ĶԻ��ߵ�Ӱ��ѧ���Ͻ��ж�����ˡ���չ����ʱ��ָ���Ǵӻ��߲μ����������Ӱ��ѧ���ٴ�����������չ�������������ȷ�����Ϊ��֮�������ʱ�䡣
�������Է�����ITT����Ⱥ���еij�����չ���������������Ӱ��ѧר�Ҹ��ˣ������ϼ���5-9���ھ�Ӱ��ѧ֤ʵ��342����չ���滼������281����Ӱ��ѧ��չ��������Ӱ��ѧר�Ҹ��ˣ���15��Ϊ�ٴ���չ��46������������δ���ּ�����չ����
��5-9���о�11213������Ӱ��ѧ֤ʵ����չ�������
��������Ⱥ�������������
|
���� |
Sorafenib�飨��384���� |
��ο���飨��385���� |
|
�ܽ�չ���� |
147��38.3%�� |
195��50.6�� |
|
��չ�������� |
237��61.7%�� |
190��49.4�� |
|
��λ��չ�����ڣ��죩 |
167 |
84 |
|
��λPFS��95%�������䣨�죩 |
139-174 |
78-91 |
|
Σ�ձȣ�Sorafenib��/��ο���飩 |
0.44��P��0.000001�� | |
|
Σ�ձȵ�95%�������� |
0.35-0.55 | |
��ο����Ļ�����λ��չ������Ϊ84�죬Sorafenib����λ��չ������Ϊ167�졣�ֲ�log-rank����˫��Pֵ��0.000001�����Ƶ�Σ�ձȣ�ָSorafenib�黼����Ȱ�ο���黼������չ��Σ���Դ�С��Ϊ0.44��95%��������CIֵΪ0.35-0.55����Ҳ����˵Sorafenib��Ļ��߱Ȱ�ο���黼������չ�ķ����½���56%��ͼ5-2��������չ�����Kaplan-Merier�������ߡ�
ͼ5-2���о�11213�о�����Ӱ��ѧ֤ʵ����չ��������
��������Ⱥ���������Ʒ�������
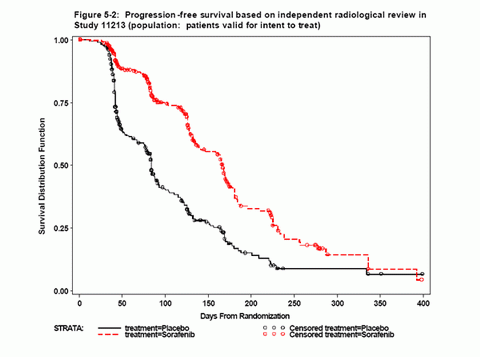 ��������3����ʱ��Sorafenib�黼����չ������Ϊ75%��95%��������Ϊ70%-80%������ο������չ������Ϊ43%��95%��������Ϊ36%-49%����6����ʱSorafenib�黼����չ������Ϊ37%��95%��������Ϊ29%-45%������ο������չ������Ϊ17%��95%��������Ϊ11%-23%��
��������3����ʱ��Sorafenib�黼����չ������Ϊ75%��95%��������Ϊ70%-80%������ο������չ������Ϊ43%��95%��������Ϊ36%-49%����6����ʱSorafenib�黼����չ������Ϊ37%��95%��������Ϊ29%-45%������ο������չ������Ϊ17%��95%��������Ϊ11%-23%�� ���˿�ͳ��ѧ�������ں�Ԥ��ָ��ȷ���Ծ�����Ӱ��ѧ֤ʵ����չ��������˷ֲ����������ÿһ�����м�����չ��Σ�ձȣ�Sorafenib��/��ο���飩����95%�������䣬Σ�ձ�С��1˵��Sorafenib��Ч��ͼ5-3�б���ÿ��������������Σ�ձȾ�����С��1��
ͼ5-3���о�11213�и����黼�ߵ���չ�������
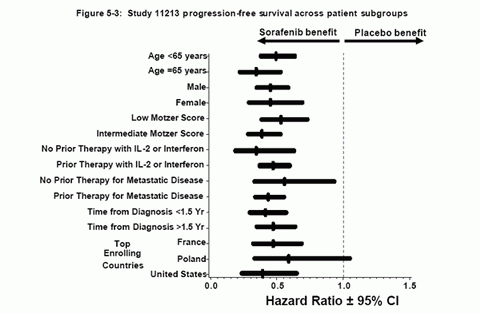

������չʱ�䣨TTP��ָ���ǻ��ߴӲμ�������鿪ʼ�����ּ�����չ�����һ�α�ȷ��������δ��չ֮���ʱ�䡣��������Ӱ��ѧ֤ʵ����λ������չʱ���ڰ�ο���黼����84�죬����Sorafenib�黼����168�죨P��0.000001��������Σ�ձȣ�Sorafenib����ο����Ϊ0.40����Sorafenib��Ļ����밲ο����Ļ�����ȼ�����չ�ķ��ս�����60%��
�ڻ����ں�ʵ�ʲμ�����������574�������У�293����Sorafenib�飬281������ο���顣��ÿһ������Ŀ�겡���С���������ֵ������������ͼ5-4�г��˻��ߴӻ����ں�������С�����ٷֱȣ�ÿһ�����ߵ����ݾ���ͼ�е�һ��ֱ����ʾ����������߲�����С��δ�ﵽʵ��������Ӧ����RECIST���еĻ����������Sorafenib�黼������74%���ֲ�ͬ�̶ȵ�������С������ο�����н���20%��
ͼ5-4���о�11213�л���Ŀ�겡�����Ӱ��ѧ֤ʵ��С�����ٷֱ�
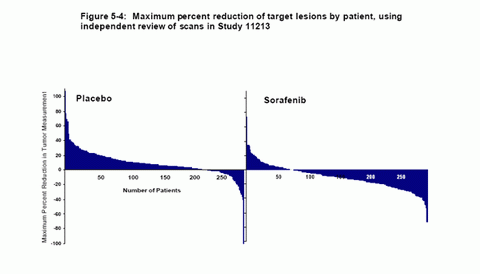

��֮���Ӵ���˫ä����ο�����յ��о��п����Եķ�ӳ������Ӧ��Sorafenib���Ƶ��ٴ������ͳ��ѧ����չ�����������ӳ������ֽ���ڻ����ڸ��ݲ�ͬ�������ֵĸ������ж���һ�µģ�����Sorafenib���й�����Ч�ԡ����Ͻ��֤����Sorafenib����������������Ч�ԡ�
TAG�� �༪�� ���� �ΰ�
���ҩƷ
����ҩ������

ʮ��ȫ������ר��ҩ����ȫ����ר������ҩ��������ȫ������ӵ����ʮλִҵҩʦ��
�ټý����̳ǡ�������ҩƷ�������ʸ�֤�顷 ��C20110003

- ר�Ʋ���������
- ������
- ���
- ��
- �����
- Ƥ���Բ���
- �ۿ�
- ��ʪ���߿�
- ����Ѫ�ܿ�
- ����
- ������ֳ��
- Ӫ��������
- ҽ����е��
- ҩƷ˵����������
- ������
- ���
- ��
- �����
- Ƥ���Բ���
- �ۿ�
- ��ʪ���߿�
- ����Ѫ�ܿ�
- ����
- ������ֳ��
- Ӫ��������
- ҽ����е��
- ��Ծ���촯����(Բ��)
- Խ
- ���������ƶ���ά����Ƭ����ʿ��
- ��ׯ�������¼�TSO-B��ͷ
- ��Ծ���γ�1100A
- ��������RҺ���������
- MiKi���γ�MSL-T 22"ʵ��̥
- ����������ţ��Ʒ�
- ���������߶��¼�TET-350
- �»������Ͻ�������HF7-09A
- ��������Rţ���鸴�Ϸ�
- Miki��̫���Ͻ��ܳ�������MCS-43L
- ӯ�����Ͻ�������м�IT601
- ��ֽ(B5)
- MiKi���γ�MPTC-46Lʵ��̥
- ������ʽ����Ѫѹ��DB31
- Miki��̫���Ͻ���������LS-1
- ��Ծ���촯����(����)
- ŷķ���������¼�MC-612
- ΰҵ���Ͻ�ʹ�
- ǿ���Ⱥ�������Ѫ���ǣ���ɫ��
- ��������ʪ�ȼ�TT-509
- Miki��̫���Ͻ����������MOCSW-43J�������
- ��Ծ�������YU870�������ʣ�
- ǿ���Ȳ���Ѫ����ֽ(50Ƭ)
- ����
- ҩƷר��������
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- ����¼
- ����¼
- ����¼
- ����¼
��վ��Ѷ- ҩ������ |
�����ŵ�ֲ� | �˲���Ƹ |
��ϵ���� | ��վ��ͼ
�������- �������� | ����ָ�� | ҩѧ���� | �˿���� | �˿�Ͷ�� | ר�Ʒ��� | Ѱҽ��ҩ | ҩʦ����
ר�Ʒ������- ������ | �β��� | �� | ����� | Ƥ���Բ��� | �� �� | ��ʪ���߿� | ��Ѫ�ܿ� | ���� | ��������ҩ
ҩƷ��������- ������ҩƷ | �����ҩƷ | �β���ҩƷ | �ۿ�ҩƷ |Ƥ���Բ���ҩƷ | ��ҩƷ | ��ʪ���߿�ҩƷ
ҩ������- ��ҵ����Ӫҵִ�� | ҩƷ��Ӫ����֤ | ҩƷ��Ӫ���������淶��֤ | ʳƷ��������֤ | ������ҩƷ��Ϣ�����ʸ�֤
�������- �������� | ����ָ�� | ҩѧ���� | �˿���� | �˿�Ͷ�� | ר�Ʒ��� | Ѱҽ��ҩ | ҩʦ����
ר�Ʒ������- ������ | �β��� | �� | ����� | Ƥ���Բ��� | �� �� | ��ʪ���߿� | ��Ѫ�ܿ� | ���� | ��������ҩ
ҩƷ��������- ������ҩƷ | �����ҩƷ | �β���ҩƷ | �ۿ�ҩƷ |Ƥ���Բ���ҩƷ | ��ҩƷ | ��ʪ���߿�ҩƷ
ҩ������- ��ҵ����Ӫҵִ�� | ҩƷ��Ӫ����֤ | ҩƷ��Ӫ���������淶��֤ | ʳƷ��������֤ | ������ҩƷ��Ϣ�����ʸ�֤







