您现在的位置: 百济新特药房网首页 >> 肝病科 >> 脂肪肝 >> 脂肪肝常规用药
09年美国肝病学会酒精性肝病诊疗指南(二)诊断及预后
- 来源: 《中华肝脏病杂志》 作者:百济动态 浏览: 发布时间:2010/9/2 2:52:00
四、ALD的诊断
ALD的诊断包括大量饮酒史、肝病的临床证据以及辅助检查的异常。指南强调,这些指标常受到患者和医生病史的采集以及实验室检测结果的限制。因为(1)否认酗酒及少报酒精摄入量在患者中很常见;(2)内科医生往往低估酒精相关问题;(3)依靠查体和实验室检查都无法诊断ALD,尤其是在轻度ALD或早期肝硬化患者。指南建议内科医生必须提高对患者可能存在ALD的警惕性以及依赖间接地酗酒证据,如对家庭成员进行问卷调查、咨询或者用实验室检验来验证或确认临床的怀疑。
ALD的诊断包括大量饮酒史、肝病的临床证据以及辅助检查的异常。指南强调,这些指标常受到患者和医生病史的采集以及实验室检测结果的限制。因为(1)否认酗酒及少报酒精摄入量在患者中很常见;(2)内科医生往往低估酒精相关问题;(3)依靠查体和实验室检查都无法诊断ALD,尤其是在轻度ALD或早期肝硬化患者。指南建议内科医生必须提高对患者可能存在ALD的警惕性以及依赖间接地酗酒证据,如对家庭成员进行问卷调查、咨询或者用实验室检验来验证或确认临床的怀疑。
(一) 酒精滥用的筛选
临床上经常由于不能有效的筛选患者,导致对酗酒诊断和治疗的失败。酒精滥用或酒精依赖的病史包括饮酒方式、类型、摄入量,以及酒精滥用导致的社会或心理问题的证据。这些可能通过其他方面的损伤或过去的创伤例如频繁跌(摔)倒、撕裂、烧伤、骨折以及急诊就诊等提示。
临床上经常由于不能有效的筛选患者,导致对酗酒诊断和治疗的失败。酒精滥用或酒精依赖的病史包括饮酒方式、类型、摄入量,以及酒精滥用导致的社会或心理问题的证据。这些可能通过其他方面的损伤或过去的创伤例如频繁跌(摔)倒、撕裂、烧伤、骨折以及急诊就诊等提示。
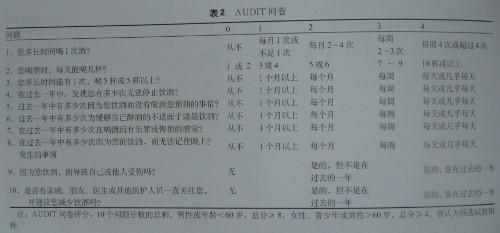
1. 问卷调查:指南认为,在酒精滥用筛查中生物化学试验不如问卷调查灵敏,后者还可鉴别是否复发。并推荐数种调查问卷,包括CAGE、密歇根酒精中毒筛查试验(MAST)以及酒精使用障碍鉴别测试(AUDIT)。结构性访问通常作为量化终身饮酒史的金标准。指南主要推荐CAGE和AUDIT两个问卷,见表1,2。

一项荟萃分析表明,CAGE问卷以超过2项阳性反应作为截断值时,发现总体敏感性和特异性分别是0.71和0.90。其优点主要是问题简单(只有四个是非选择题),并可以包含在病史内作为书面文档自我管理,由于他的长期实用性,仍用于大范围的人群测试;缺点主要是注重摄入酒精的后果而不是实际饮用的酒精量,以及它反应行为的终身模式,而不是短期或最近的改变。
AUDIT可避免种族和文化的偏倚,它有更高的敏感性和特异性(初期调查的敏感性波动在51%-97%,特异性波动在78%-96%)。具有3个优点:可以区分还未发展为酒精依赖的“危险”饮酒者;包括了饮酒量的测定;还包括现在和终身的饮酒时间间隔。他可能在明确的酒精依赖或酗酒被诊断前就发现饮酒的问题,因此在不同人群可能更有力和更有效。AUDIT评分>8或者超过1d的大量饮酒,则筛查试验阳性,提示需进一步评估以排除酒精滥用。
AUDIT可避免种族和文化的偏倚,它有更高的敏感性和特异性(初期调查的敏感性波动在51%-97%,特异性波动在78%-96%)。具有3个优点:可以区分还未发展为酒精依赖的“危险”饮酒者;包括了饮酒量的测定;还包括现在和终身的饮酒时间间隔。他可能在明确的酒精依赖或酗酒被诊断前就发现饮酒的问题,因此在不同人群可能更有力和更有效。AUDIT评分>8或者超过1d的大量饮酒,则筛查试验阳性,提示需进一步评估以排除酒精滥用。
2. 血清生物化学指标检测:长期使用酒精的血清标志物中,指南推荐①γ~谷氨酰转肽酶(GGT),它可以为诊断酒精滥用以及饮酒问题提供独立信息。然而,低灵敏度和特异性限制了GGT诊断酒精滥用的有效性,GGT的水平可以随大面积肝损伤而波动。低水平的GGT(<100U/L)或者总胆红素/GGT>1,已作为酒精性肝硬化患者1年病死率的预测因子。②平均红细胞体积(MCV),酗酒者可出现巨红细胞症,但其敏感性低,结合GGT可能会提高诊断酒精滥用的敏感性。③糖缺失转铁蛋白,但其敏感性和特异性有限,它的试验特性也受年龄、性别、体重指数以及其他慢性肝病等因素的影响。指南提示,由于单一指标往往缺乏敏感性和特异性,所以尽量避免依据某种单一的生物化学指标进行评价。
(二) 查体
ALD患者的查体可能出现从正常到进展性肝硬化。由于ALD可能与其他慢性肝病同时存在,所以其体格检查的敏感性通常较低,即使在进展期肝病及肝硬化等有明显体征的阶段,查体的特征性表现也缺乏特异性。肝脏体积大小不一定能提供正确的信息,而且通常是正常的。腮腺体、掌挛缩、伴随女性化在ALD更常见,但都缺乏特异性和敏感性。一些查体的特征可能会提示一些预后的信息,特异性体征的表现可能与1年期病死率的增加有关,如肝性脑病(相关的风险为4.0)、前腹壁静脉显露(2.2)、浮肿(2.9)、腹水(4.0)、蜘蛛痣(3.3)、乏力(2.1)等。AH时有极少数病例(4/240)在肝脏表面可听到杂音,但指南建议谨慎地采纳这个查体的诊断标准。
指南提醒内科医生需要意识到ALD不是单独存在的,它可能与酒精滥用所致的其他器官功能不全共存,包括心肌病、骨骼肌溶解、胰腺功能不全以及酒精性神经损伤等。在查体中必须寻找这些证据,以便提供更合适的治疗。
ALD患者的查体可能出现从正常到进展性肝硬化。由于ALD可能与其他慢性肝病同时存在,所以其体格检查的敏感性通常较低,即使在进展期肝病及肝硬化等有明显体征的阶段,查体的特征性表现也缺乏特异性。肝脏体积大小不一定能提供正确的信息,而且通常是正常的。腮腺体、掌挛缩、伴随女性化在ALD更常见,但都缺乏特异性和敏感性。一些查体的特征可能会提示一些预后的信息,特异性体征的表现可能与1年期病死率的增加有关,如肝性脑病(相关的风险为4.0)、前腹壁静脉显露(2.2)、浮肿(2.9)、腹水(4.0)、蜘蛛痣(3.3)、乏力(2.1)等。AH时有极少数病例(4/240)在肝脏表面可听到杂音,但指南建议谨慎地采纳这个查体的诊断标准。
指南提醒内科医生需要意识到ALD不是单独存在的,它可能与酒精滥用所致的其他器官功能不全共存,包括心肌病、骨骼肌溶解、胰腺功能不全以及酒精性神经损伤等。在查体中必须寻找这些证据,以便提供更合适的治疗。
(三) 实验诊断
ALD的诊断是建立在过量饮酒以及存在肝病的基础上。没有单一的生物标记能够明确的判定究竟是肝损伤的病因。对于一个多因素导致肝损伤的患者,很难评价酒精单独起的作用,它可能是引起肝损伤系列因素中的一个。
对于重型AH患者,指南强调血浆AST的重要性。重型AH时,AST升高,达正常值上限的2-6倍,但很少超过500U/L或者ALT>200U/L,一旦超过常提示可能存在其他病因(如对乙酰氨基酚过量)。大约70%的患者AST/ALT>2,在无肝硬化的患者中可能更高,AST/ALT>3更能提示ALD。
ALD的诊断是建立在过量饮酒以及存在肝病的基础上。没有单一的生物标记能够明确的判定究竟是肝损伤的病因。对于一个多因素导致肝损伤的患者,很难评价酒精单独起的作用,它可能是引起肝损伤系列因素中的一个。
对于重型AH患者,指南强调血浆AST的重要性。重型AH时,AST升高,达正常值上限的2-6倍,但很少超过500U/L或者ALT>200U/L,一旦超过常提示可能存在其他病因(如对乙酰氨基酚过量)。大约70%的患者AST/ALT>2,在无肝硬化的患者中可能更高,AST/ALT>3更能提示ALD。
(四) 肝脏影像学
指南指出,超声、CT以及磁共振等常用于诊断肝病,均可提示脂肪变性、肝硬化以及肝细胞癌的诊断,不能确定酒精作为肝病特异性病因,但可以排除酒精滥用患者肝脏异常的其他原因,例如胆管梗阻以及肝脏浸润性或肿瘤性疾病。影像学提示酒精性肝硬化的特异性表现包括尾状叶增大、肝右后叶切迹,与病毒性肝炎相比,酒精性肝硬化的再生结节更小。
指南指出,超声、CT以及磁共振等常用于诊断肝病,均可提示脂肪变性、肝硬化以及肝细胞癌的诊断,不能确定酒精作为肝病特异性病因,但可以排除酒精滥用患者肝脏异常的其他原因,例如胆管梗阻以及肝脏浸润性或肿瘤性疾病。影像学提示酒精性肝硬化的特异性表现包括尾状叶增大、肝右后叶切迹,与病毒性肝炎相比,酒精性肝硬化的再生结节更小。
(五) 肝脏或组织检查
肝脏或组织检查在ALD的诊断中并不是必须的,但有助于判断肝病的病因,因为超过20%有酒精滥用史的患者常存在次要的或共存的其他肝病病因,而且有益于确定ALD的分期和严重性。
组织学特征主要取决于损伤的程度和范围。包括脂肪变性、小叶增生、汇管区纤维化、Mallory小体、细胞核空泡变性、胆管增生以及纤维化或硬化。这些在同一张切片中可能共存,然而都不能单独地作为ALD特征性改变。AH的组织学可能有特异的组织学表现,包括融合结节坏死、脂肪变性、核周和细胞周围胶原沉积、气球样变以及在早期即有静脉周围的炎症。肝脏可能有多形核白细胞浸润和Mallory小体。
组织学特异性的表现也有助于预后的判断。多形核白细胞浸润程度、胆汁淤积等提示ALD预后不良。巨大线粒体的出现可能提示为轻型AH,肝硬化和并发症的发生率较低,具有良好的长期生存率。静脉周围和细胞周围纤维化,预示AH可能会发展至肝硬化,尤其在继续饮酒或者合并丙型肝炎病毒感染者,还可预测严重AH使用皮质类固醇治疗的反应。
指南同时指出,如果无需进行对ALD或AH的治疗,应用无创性检查即可对患者的预后进行评估,通常就不需要组织学诊断;相反,如果需要设计一个实验性的治疗,或进行具有风险性的治疗,那么就要进行肝脏或组织检查的风险/获益比的判定。
肝脏或组织检查在ALD的诊断中并不是必须的,但有助于判断肝病的病因,因为超过20%有酒精滥用史的患者常存在次要的或共存的其他肝病病因,而且有益于确定ALD的分期和严重性。
组织学特征主要取决于损伤的程度和范围。包括脂肪变性、小叶增生、汇管区纤维化、Mallory小体、细胞核空泡变性、胆管增生以及纤维化或硬化。这些在同一张切片中可能共存,然而都不能单独地作为ALD特征性改变。AH的组织学可能有特异的组织学表现,包括融合结节坏死、脂肪变性、核周和细胞周围胶原沉积、气球样变以及在早期即有静脉周围的炎症。肝脏可能有多形核白细胞浸润和Mallory小体。
组织学特异性的表现也有助于预后的判断。多形核白细胞浸润程度、胆汁淤积等提示ALD预后不良。巨大线粒体的出现可能提示为轻型AH,肝硬化和并发症的发生率较低,具有良好的长期生存率。静脉周围和细胞周围纤维化,预示AH可能会发展至肝硬化,尤其在继续饮酒或者合并丙型肝炎病毒感染者,还可预测严重AH使用皮质类固醇治疗的反应。
指南同时指出,如果无需进行对ALD或AH的治疗,应用无创性检查即可对患者的预后进行评估,通常就不需要组织学诊断;相反,如果需要设计一个实验性的治疗,或进行具有风险性的治疗,那么就要进行肝脏或组织检查的风险/获益比的判定。
五、预后的评估
有关预后评估的方法主要是针对AH。指南主要推荐的评估方法是Maddrey判别函数(maddrey discriminant function,MDF),MDF=4.6x(患者的凝血酶原时间-对照凝血酶原时间)+总胆红素(mg/dl)。患者的MDF评分≥32处于死亡的高风险,1各月内的病死率高达30%-50%,尤其合并有肝性脑病者将处于最高的风险。这是评估患者预后的一个动态模型,它随时间的推移实验室结果将发生变化,包括入院后第一周胆红素的变化,与用氢化波尼松治疗AH患者的预后有明显相关。
推荐的其他常用的评分系统包括MELD评分、Glasgow AH评分、CTP评分和Lille model-PT模型,包括MDF均可在互联网(www.lillemodel.com)上自动获取这些模型的结果。由于内在的取舍,包括设定实验阈值、最佳截断值(切点)等对于每一个评分系统的指数都没有明确的设定。一些调查者推荐这些指数的判断界值,包括MDF≥32、MELD评分>11、GAHS评分>8,提示患者预后不良。作为预后不良高风险患者早期诊断的目标,需要一个敏感型最大的测试,使用MDF(截断值为32和/或肝性脑病的出现)选择患者的治疗似乎比较合理。
有关预后评估的方法主要是针对AH。指南主要推荐的评估方法是Maddrey判别函数(maddrey discriminant function,MDF),MDF=4.6x(患者的凝血酶原时间-对照凝血酶原时间)+总胆红素(mg/dl)。患者的MDF评分≥32处于死亡的高风险,1各月内的病死率高达30%-50%,尤其合并有肝性脑病者将处于最高的风险。这是评估患者预后的一个动态模型,它随时间的推移实验室结果将发生变化,包括入院后第一周胆红素的变化,与用氢化波尼松治疗AH患者的预后有明显相关。
推荐的其他常用的评分系统包括MELD评分、Glasgow AH评分、CTP评分和Lille model-PT模型,包括MDF均可在互联网(www.lillemodel.com)上自动获取这些模型的结果。由于内在的取舍,包括设定实验阈值、最佳截断值(切点)等对于每一个评分系统的指数都没有明确的设定。一些调查者推荐这些指数的判断界值,包括MDF≥32、MELD评分>11、GAHS评分>8,提示患者预后不良。作为预后不良高风险患者早期诊断的目标,需要一个敏感型最大的测试,使用MDF(截断值为32和/或肝性脑病的出现)选择患者的治疗似乎比较合理。
TAG:酒精性肝病 美国肝病学会 脂肪肝 肝纤维化 肝硬化
相关药品








