您现在的位置: 百济新特药房网首页 >> 行业资讯 >> 新药快讯
重磅! 复星凯特CAR-T产品阿基仑赛注射液获批上市!
- 来源: 百济药房药讯 作者:百济动态 浏览: 发布时间:2021/6/23 17:17:00
2021年06月22日,复星凯特生物科技有限公司提交的阿基仑赛注射液(又称阿基仑赛,代号:FKC876)的上市申请(受理号:CXSS2000006)已被中国国家药品监督管理局(NMPA)正式批准上市,这也是国内的一个获批上市的CAR-T疗法。

图片来源:NMPA官网
2020年2月,复星凯特在中国提交了阿基仑赛注射液用于治疗既往接受二线或以上系统性治疗后复发或难治性大B细胞淋巴瘤成人患者,包括弥漫性大B细胞淋巴瘤非特指型(DLBCL,NOS),原发纵隔大B细胞淋巴瘤(PMBCL)、高级别B细胞淋巴瘤和滤泡性淋巴瘤转化的DLBCL的上市申请。


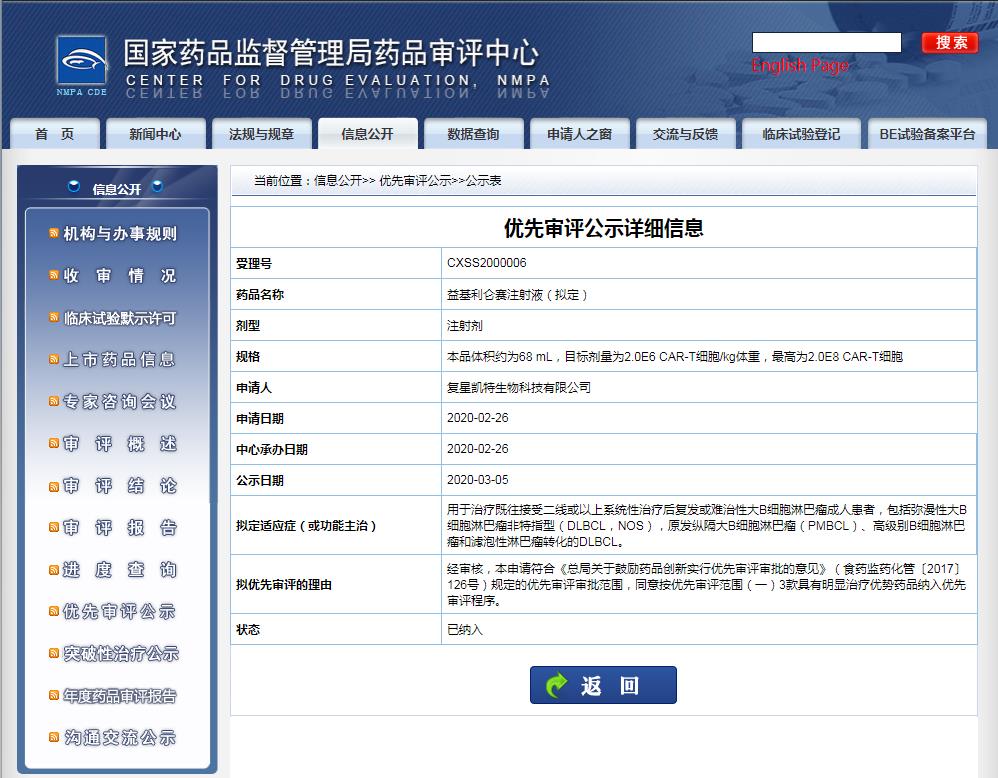
图片来源:CDE官网
2020年3月5日,复星凯特在中国提交的阿基仑赛注射液的上市申请被国家药品监督管理局药品审评中心(CDE)纳入优先审评。
阿基仑赛注射液是复星凯特于2017年初从吉利德子公司Kite制药引进的靶向CD19的基因修饰自体CAR-T细胞注射液,并获得全部技术授权。2017年10月,阿基仑赛注射液(商品名:Yescarta)获得美国食药监局(FDA)批准,并于美国上市。
2018年8月,Yescarta获得欧洲EMA批准,并于欧洲上市。2021年3月,Yescarta用于治疗之前接受过二线及以上全身治疗的复发或难治性滤泡性淋巴瘤(FL)成人患者的适应症获得美国FDA加速批准。
关于滤泡性淋巴瘤(FL)
滤泡性淋巴瘤(FL)大概占全球新确诊淋巴瘤的22%,是全球比较常见的淋巴瘤类型,当前依然无明确的标准治疗方案。
近年来,随着新药的上市,滤泡性淋巴瘤患者的生存期一般能得到延长。但是,患者通过治疗后,仍然容易面临再次复发的风险,预后较差。
目前,对于一些可能已经用尽可用方案但是依然健康可以接受积极治疗的患者、以及对方案难治或很快复发的患者来说,需求尚未得到满足。
祝贺复星凯特CAR-T疗法正式获批在中国获批上市,为患者带来更多治疗希望和机会。








